Осложнения беременности: все о возможных генетических рисках

Осложнения во время беременности — страх, преследующий многих будущих матерей. И опасения столкнуться с ними вполне понятны, ведь они угрожают жизни и здоровью не только ребенка, но и самой женщины.
Однако, знание о таких патологиях позволяет предотвратить их появление или уменьшить (насколько это возможно) их последствия, если они уже имеются.
Из этой статьи вы узнаете, какие именно риски сопутствуют вынашиванию и рождению ребенка, что их вызывает и как с ними бороться.
Что такое осложнение беременности?
Под осложненной беременностью в гинекологии и акушерстве понимается состояние организма матери и/или плода, несущее угрозу их жизни и здоровью.
Оно может быть связано как с патологиями самой репродуктивной системы и эмбриона, так и с негинекологическими заболеваниями у женщины.
[attention type=yellow]В зависимости от вида осложнений, они могут развиваться и проявляться на различных стадиях беременности и родов.
[/attention]Такие патологии могут спровоцировать самые разнообразные последствия для женщины и ее ребенка:
- физические и психические аномалии развития малыша;
- потерю плода (выкидыш);
- невозможность последующего зачатия и успешного вынашивания ребенка;
- депрессию и страх будущих беременностей у женщины;
- смерть матери.
Очевидно, что такой перечень последствий делает вопрос о наличии осложнений при беременности чрезвычайно важным. Если у будущей матери в результате обследований обнаружились риски, ей должна быть оказана вся необходимая медицинская помощь для сохранения здоровья и жизни ее самой и (по возможности) будущего ребенка.
Возможные осложнения беременности
К сожалению, патологии во время беременности — достаточно частое явление. Ежегодно около 800 женщин по всему миру погибает от них, гораздо больше наблюдается случаев, не вызывающих летального исхода, но несущих тот или иной вред здоровью матери или ребенка. К наиболее частым осложнениям беременности относятся следующие патологии:
- Гестоз (токсикоз). Характеризуется нарушением работы органов и систем материнского организма. Гестозы являются одной из основных причин материнской смертности в развитых странах. Это осложнение проявляется такими симптомами, как рвота, слюнотечение, отеки, нефропатиями (нарушениями работы почек), эклампсией (судорогами), реже — потерей веса, ухудшением состояния кожи, сосудов, нервной ткани и т. д. Точные причины данной патологии неизвестны, различные теории связывают ее с эндокринными, генетическими, психическими, аутоиммунными расстройствами.
- Угроза прерывания беременности. Проявляется высоким риском раннего отторжения плода (выкидыша). Это осложнение беременности является одним из самых распространенных и может возникать по разным причинам, чаще всего им страдают те, у кого уже были выкидыши в анамнезе. По статистике, 15-20% беременностей заканчиваются самопроизвольным абортом. Данная патология однозначно ведет к смерти ребенка. Последствия для матери могут варьироваться от психологического стресса до бесплодия и даже смерти — например, от развившихся при отсутствии должной медицинской помощи инфекций.
- Замершая беременность. Это осложнение также именуется скрытым абортом и заключается во внутриутробной гибели плода на ранней стадии беременности (до 20 недели). При этом отчетливых симптомов не проявляется, патология обнаруживается при рутинном обследовании. Последствия замершей беременности могут быть различными — самопроизвольный выкидыш, интоксикация материнского организма продуктами распада плода. В редких случаях наблюдается окаменение мертвого эмбриона (литопедион). Чаще всего после выявления замершей беременности назначается искусственное удаление плода и околоплодных оболочек.
- Гипертензия беременных. Это повышение артериального давления в период вынашивания, протекающее бессимптомно или проявляющееся головной болью, слабостью, тошнотой, нарушениями сна, головокружением и т. д. Гипертензия представляет серьезную опасность как для самой матери, так и для ребенка. В частности, она может вызвать выкидыш, гипоксию эмбриона, отслойку плаценты и другие нарушения.
- Гипоксия плода. Под ней понимается недостаточное поступление кислорода к органам и тканям плода. В зависимости от тяжести патологии, она может вызвать смерть эмбриона или тяжелые нарушения его физического и психического развития. Гипоксия развивается на любом сроке беременности, может быть кратковременной, острой или хронической. К ее появлению приводит множество причин — заболевания матери, передавливание кровяного русла плода, многоплодие, повреждение матки и т. д.
- Многоплодная беременность. Не является патологией в прямом смысле этого слова, но считается аномалией и требует более строго наблюдения. При многоплодной беременности женщина вынашивает сразу несколько эмбрионов, что повышает нагрузку на организм. Из возможных негативных последствий этого осложнения можно упомянуть анемию, многоводие, чрезмерную рвоту, отслойку нормально расположенной плаценты, артериальную гипертензию, преждевременные роды со стороны матери и недоношенность, внутриутробную гибель одного из близнецов, задержку и другие аномалии развития со стороны плода.
- Резус-конфликт. Эта патология заключается в иммунном ответе материнского организма на наличие в нем плода с противоположным резус-фактором. Иными словами, иммунитет женщины распознает эмбрион как инородное тело и старается от него избавиться с помощью защитных антител. Резус-конфликт может привести к поражениям плода различной тяжести — от анемии и желтухи до водянки и синдрома отечности плода, которые способны спровоцировать мертворождение.
- Фето-фетальный трансфузионный синдром. Патология возникает при многоплодной беременности у близнецов с одной плацентой с существенно разным кровотоком. При образовании сосудов, соединяющих кровяное русло плодов, кровь может перетекать от одного к другому, вызывая диспропорцию в кровоснабжении. Это приводит к гипоксии, маловодию, поражениям выделительной системы, задержкам развития у эмбриона-донора и многоводию, высокой нагрузке на сосудистую систему у эмбриона-рецепиента. ФФТС является тяжелым осложнением, смертность при котором может достигать 60-100%.
Существует множество других осложнений беременности, непосредственно связанные с репродуктивной системой матери и плодом. В частности, распространенно тазовое предлежание плода, затрудняющее или делающее невозможным его естественный выход из половых путей при родах.
Среди более экзотических патологий можно отметить синдром “эмбрион в эмбрионе”, возникающий при многоплодной беременности, когда в процессе развития один из близнецов “поглощает” второго, развитие которого останавливается и он становится неспособным жить вне организма брата.
К осложнениям беременности также относятся патологии общего характера.
Среди них можно упомянуть инфекционные заболевания (в том числе передающиеся половым путем), врожденные аномалии органов и систем матери, различные эндокринные нарушения, расстройства обмена веществ.
Варикозное расширение вен нижних конечностей и влагалища, сахарный диабет, туберкулез, порок сердца и прочие общие патологии способны повлиять на физическое и психическое развитие ребенка, а также на здоровье женщины.
Факторы, приводящие к осложнениям беременности
Осложнения во время беременности появляются по самым различным причинам. К наиболее значимым из них относятся:
- Генетические нарушения. Этот фактор может носить как случайный, так и наследственный характер. В первом случае подразумевается патология генов плода, появившаяся в результате их случайной рекомбинации из геномов здоровых родителей в момент оплодотворения. Наследственные генетические нарушения передаются эмбриону от его матери и отца, при этом в семье они могут наблюдаться в течение нескольких поколений. Например, наличие родственников с задержкой умственного развития повышает генетический риск осложнения беременности с патологией плода аналогичного характера.
- Инфекции. Вирусные, бактериальные, грибковые заболевания — частая причина патологий, возникающих во время беременности. Попадая в организм матери, инфекционные возбудители провоцируют иммунный ответ, который может воздействовать и на ребенка. Сами они также оказывают негативное влияние на здоровье плода, причем на всех стадиях его развития — от зачатия до родов. Инфекции могут вызывать различные патологические явления в репродуктивной системе женщины, мешающей ей нормально зачать, выносить и родить здорового малыша.
- Заболевания различной природы. Помимо инфекций, негативно повлиять на протекание беременности могут другие врожденные и приобретенные патологии. Сахарный диабет, высокое артериальное давление (гипертензия), аномалии развития органов репродуктивной системы, заболевания сердца и сосудов, почек, печени, доброкачественные и злокачественные новообразования, психические нарушения часто приводят к выкидышам, физической или психической неполноценности рожденного ребенка.
- Вредные привычки. Употребление алкоголя и наркотических веществ (особенно систематическое), курение одного или обоих родителей — еще один распространенный фактор, вызывающий патологии беременности. Этиловый спирт, психотропные вещества, никотин, а также находящиеся в составе спиртных напитков, сигарет и наркотиков примеси обладают канцерогенным и тератогенным действием. Помимо непосредственного риска выкидыша или замершей беременности, они оказывают долгосрочные эффекты, которые могут проявиться у ребенка в подростковом или взрослом возрасте. Одним из самых частых таких последствий является алкогольный синдром плода, проявляющийся в задержке умственного развития, лицевые дефекты, антисоциальное поведение.
- Прием лекарственных препаратов. Осложнить зачатие, вынашивание и роды могут медикаменты, которые принимает женщина в период вынашивания ребенка. К сожалению, многие лекарства имеют выраженный тератогенный эффект, который необходимо учитывать при их назначении. При выпуске каждого препарата предусмотрены его клинические испытания на выявление побочных воздействий на плод. Проблема в том, что далеко не все производители фармацевтики проводят полноценные тесты на тератогенность. Например, широко известна история со снотворным “Талидомид”, который в середине прошлого века привел к массовым случаям рождения детей с аномалиями развития в США.
- Возрастные изменения. Оптимальный возраст для вынашивания здорового ребенка — 20-35 лет. В этот период репродуктивная система женщины наиболее активна, а сама будущая мама психологически подготовлена к беременности. Более ранний и поздний срок наступления беременности существенно повышает риск выкидыша или рождения ребенка с пороками развития. Так, зачатие после 35 лет увеличивает вероятность появления малыша с синдромом Дауна. Ранняя беременность также несет определенные риски, связанные с незрелостью репродуктивной системы будущей мамы.
- Социальное положение. На течение беременности оказывает влияние условия, в которых живет будущая мама. Низкое социальное положение, тяжелая работа, недоедание повышают физическую и эмоциональную нагрузку на женщину. Малый финансовый доход ограничивает ее доступ к современной медицине, заставляет трудиться в период вынашивания, в том числе заниматься предоставлением сексуальных услуг за деньги. Кроме того, часто матери живут в антисанитарных условиях, где велика вероятность заболеть инфекцией.
Среди прочих факторов, повышающих риск осложнения беременности, можно упомянуть неблагоприятную экологическую обстановку, сильный и/или постоянный эмоциональный стресс, случайно или намеренно нанесенные (в том числе посторонними лицами) травмы, нерациональное питание и т. д. Эти причины могут наблюдаться у конкретной женщины как по-отдельности, так и в комплексе — во втором случае существенно усложняется диагностика патологий.
Выявление и профилактика осложнения беременности
Определение рисков патологий — важнейшая составляющая программы ведения беременности.
В ходе обследования врач выявляет у будущей матери факторы, способствующие осложнению, и присваивает каждому из них балл.
После этого, по совокупности результатов, он определяет степень риска для женщины и ее ребенка, на основании чего в дальнейшем выстраивается стратегия по сохранению или прерыванию беременности.
Важную роль в процессе определения рисков играет сбор анамнеза у будущей матери. Таким образом выявляются следующие факторы:
- наличие патологий беременности в прошлом — в частности, имевшиеся ранее выкидыши серьезно повышают шансы на самопроизвольный аборт в текущий период вынашивания;
- генетический риск осложнения беременности — наличие у родителей родственников с наследственными заболеваниями также является причиной для более строго наблюдения за состоянием матери и плода;
- перенесенные и имеющиеся общие заболевания — сбор сведений о них от самой пациентки позволяет ускорить обследование, что особенно полезно в случаях, когда требуется экстренная помощь.
Безусловно, помимо сбора данных от самой матери, врач осуществляет комплексное медицинское обследование (скрининг), включающее следующие тесты:
- ультразвуковое исследование;
- генетический ДНК-тест;
- лабораторный анализ мочи и крови (на гормоны, антитела);
- тест на наличие инфекций;
- биопсию хориона, околоплодной жидкости и другие анализы.
Базовый набор обследований включает УЗИ и лабораторные анализы мочи и крови. При высоком риске нарушений назначаются дополнительные, в том числе инвазивные процедуры, такие как биопсия. Однако их применяют только в сложных ситуациях, так как такие методы сами способны привести к осложнениям беременности и патологиям плода.
Заключение
По статистике, более половины женщин сталкиваются с осложнениями в период вынашивания ребенка. Печальный факт в том, что абсолютно здоровая беременность — достаточно редкое явление даже в развитых странах.
Современная медицина не способна защитить будущих матерей от всех рисков.
Однако, с ее помощью можно серьезно снизить вероятность возникновения патологий или контролировать протекание беременности при уже имеющихся нарушениях и заболеваниях, дав шанс даже женщинам со слабым здоровьем выносить и родить здорового ребенка.
Источник: https://www.unona-clinic.ru/patient/articles/176/
Риск развития заболевания
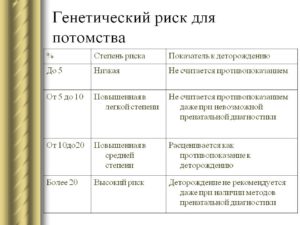
Риск развития заболевания – это вероятность возникновения заболевания на любом этапе жизни пациента. Так как болезнь может проявляться у разных людей на разных этапах жизни, чаще всего риск рассчитывают как среднюю вероятность развития данного заболевания в популяции. В таком случае мы имеем дело с относительным риском развития заболевания.
Относительный риск рассчитывается путем сравнения рисков развития данного заболевания в группе людей, обладающих каким-либо общим признаком (к примеру, это могут быть пациенты с высоким уровнем холестерина — известного фактора риска развития ишемической болезни сердца или носители определенного генотипа какого-либо гена) и в контрольной группе, в которую входят люди случайным образом выбранные из общей популяции.
Допустим, риск развития данного заболевания в изучаемой группе выше чем в общей популяции в 1,5 раза. Это значит, что страдать от ишемической болезни сердца будет, предположительно, на 50% больше людей с высоким холестерином по сравнению с людьми из общей популяции.
Такой процент не абсолютно точен, то есть, если наблюдать в течение жизни за людьми из выбранных групп, можно обнаружить что болезнь возникнет, к примеру, у 52% пациентов из группы с высоким холестерином.
Такая разница может объясняться разного рода причинами, одна из которых — размер сравниваемых групп. Чем больше людей в группе, тем больше точность определения риска.
Важно понимать, что полученный при сравнении групп риск развития заболевания относится к статистическим понятиям, так что индивидуальный риск развития для конкретного пациента и риск, подсчитанный для группы, в целом могут отличаться.
Создание модели расчета совокупного генетического риска включает два шага: 1) преобразование значения отношения шансов (OR – odds ratio) для конкретного полиморфного локуса в значение относительного риска и 2) вычисление значения совокупного относительного риска на основе значений рисков для локусов предрасположенности из первого шага.
Что такое отношение шансов (OR)?
Большая часть современных исследований генетической предрасположенности к многофакторным заболеваниям проводится с использованием подхода «случай-контроль». Задачей исследований является поиск аллелей генов, частоты которых значимо различаются в группах пациентов и здоровых индивидов.
Результаты обычно бывают представлены в виде отношения шансов (OR – odds ratio), значение которого представляет собой отношение шансов события в одной группе к шансам события в другой группе, или отношение шансов того, что событие произойдет, к шансам того, что событие не произойдет, то есть, выражаясь в терминах вероятностей:
OR = (Pr(c|A)/Pr(nc|A)) / (Pr(c|C)/Pr(nc|C))
Абсолютный риск возникновения заболевания, как правило, не может быть прямо измерен в исследованиях «случай-контроль», потому что соотношение пациентов и здоровых индивидов не соответствует их соотношению в популяции. Но, принимая некоторые допущения, мы можем оценить риск исходя из значений отношения шансов.
Известно, что для редких болезней относительный риск может быть аппроксимирован отношением шансов. В общем случае это допущение неверно для большинства распространенных многофакторных заболеваний. Однако, оказывается, что риск для генотипов может быть оценен из выражения отношения шансов, приведенного выше.
Эти вычисления особенно упрощаются, если допустить, что здоровые индивиды являются случайной выборкой из той же самой популяции, что и пациенты, включая возможно заболевших людей, а не специально отобранной группой.
Для увеличения размера выборки и статистической мощности исследования современные работы по полно-геномному поиску ассоциаций используют выборку здоровых индивидов, которая не соответствует пациентам по возрастным критериям и не гарантирует отсутствие заболевания у членов этой группы.
[attention type=red]То есть, она максимально корректно описывает случайную выборку из общей популяции. Следует отметить, что данное допущение чрезвычайно редко выполняется точно, но полученная оценка риска обычно довольно умеренна и смягчает отклонения от данного предположения.
[/attention]Исходя из этих предположений мы получаем возможность вычисления генетического риска для носителей предрасполагающего генотипа данного полиморфного маркера по отношению к среднему риску возникновения заболевания в популяции.
Как учитывать влияние нескольких полиморфных маркеров?
Для множества исследований последних лет было обнаружено, что мультипликативная модель риска адекватно описывает полученные данные и лучше подходит для описания результатов, чем альтернативные модели – доминантная и рецессивная. Это означает, что совокупный риск возникновения заболевания представляет собой произведение оценок риска для отдельных маркеров, то есть для маркеров g1 и g2:
RR(g1,g2) = RR(g1)RR(g2)
При этом подразумевается допущение, что факторы риска независимы. Очевидным нарушением этого допущения является случай неравновесия по сцеплению нескольких маркеров. В этом случае для оценки риска используются комбинации аллелей этих маркеров.
Расчет совокупного риска возникновения заболевания
Совокупный риск возникновения заболевания рассчитывается исходя из значений совокупного генетического риска для данной популяции и общего риска заболевания для популяции, представителем которой является исследуемый индивидуум (этническая принадлежность, пол, географическое происхождение и т.д.)
Таким образом, для оценки риска возникновения заболевания для конкретного пациента по сравнению со средним риском в популяции необходимо знание следующих исходных данных:
- Частоты аллелей и генотипов исследуемых полиморфных маркеров в популяции, которой принадлежит пациент
- Значения OR для исследуемых полиморфных маркеров и заболевания
- Значение популяционного риска возникновения заболевания
Краткий обзор моделей наследования
Историю развития генетического анализа можно прочитать здесь, а ниже приведен краткий перечень основных моделей наследования и связанных с ними определений и допущений, которые используются для расчета генетического риска возникновения заболевания:
Определения и допущения:
- r «случаев» и s «контролей» являются случайно отобранными образцами из популяции.
- Биаллелельный полиморфный маркер (SNP) имеет два аллеля A и B, три генотипа AA, AB и BB, где Pr(B) = pи Pr(A) = 1-p.
- Получены данные генотипирования для всех n = r + s.
- Неизвестный локус предрасположенности к болезни имеет аллели M и N.
- Исследование обнаруживает ассоциацию между заболеванием и полиморфным маркером благодаря неравновесию по сцеплению между исследуемым полиморфным маркером и локусом предрасположенности к заболеванию:
Локус предрасп. Маркер M N Всего A (1-p)(1-q) + D (1-p)q — D 1-p B p(1-q) — D pq + D p Всего 1-q q 1 - Пусть G0 = AA, G1 = AB и G2 = BB.
- Данные исследования могут быть представленны в виде таблицы сопряженности 2×3:
| G0 | G1 | G2 | Всего | |
| случаи | r0 | r1 | r2 | r |
| контроли | s0 | s1 | s2 | s |
| Всего | n0 | n1 | n2 | n |
- pi = Pr(Gi|случаи)
- qi = Pr(Gi|контроли)
- Нулевая гипотеза H0: pi = qi для i = 0,1,2
- Распространенность: k = Pr(случаи)
- Пенетрантность: fi = Pr(случаи|Gi) для i = 0,1,2
- Относительные риски для генотипов (GRR): λ1 = f1/f0 и λ2 = f2/f0
- Аллель B является предрасполагающим аллелем, если: λ2 ≥ λ1 ≥ 1 и λ2 > 1
Базовые генетические модели (m – аллель риска):
- Доминантная – предполагает, что влияние на пенетрантность проявляется для гетерозигот и гомозигот по предрасполагающему аллелю;λ1 = λ2;Pr(случаи|AB) = Pr(случаи|BB);Статистика: mm+Mm против MM (хи-квадрат).
- Рецессивная – предполагает, что влияние на пенетрантность проявляется только для гомозигот; λ1 = 1 and λ2 > 1; Pr(случаи|AA) = Pr(случаи|AB);Статистика: MM+Mm против mm (хи-квадрат).
- Мультипликативная – предполагает, что пенетрантность зависит от количества копий предрасполагающего аллеля; λ1 = λ21/2; Pr(случаи|AA) Pr(случаи|BB) = {Pr(случаи|AB)}2;Статистика: M против m (хи-квадрат).
- Аддитивная – предполагает, что значение пенетрантности гетерозигот лежит между значениями пенетрантности для обеих гомозигот; λ1 = (1+λ2)/2; Pr(случаи|AA) + Pr(случаи|BB) = 2Pr(случаи|AB);Статистика: MM против Mm против mm (тест Кохрана-Армитаджа для линейных трендов).
- Кодоминантная – предполагает, что значение пенетрантности гетерозигот лежит между значениями пенетрантности для обеих гомозигот, но зависимость от значений рисков гомозигот неизвестна; Статистика: логистическая регрессия.
По материалам проекта deCODEme
Источник: Ген Эксперт
Источник: https://testgen.ru/ru/nauchnyie-issledovaniya/publikaczii/risk-razvitiya-zabolevaniya.html
Генетический риск осложнений беременности и патологии плода

При планировании беременности женщина узнает о том, сколько обследований ей придётся пройти и сколько анализов сдать.
Некоторые будущие мамочки считают большую часть исследований напрасной тратой сил, времени и денег. Особой критике подвергается генетическая диагностика, вероятнее всего, потому что ее результаты наименее понятны.
Не понятно и что нужно предпринимать, если эти результаты свидетельствуют о высоких рисках.
Сегодня в рамках нашей статьи мы немного поговорим о том, для чего нужна диагностика генетических рисков. Что такое генетический риск осложнений беременности и патологии плода, какие осложнения могут возникать в гестационном периоде, к каким патологиям внутриутробного развития они приводят и в каких случаях их назначают.
Когда нужна генетическая диагностика?
Сегодня, в связи с ростом числа генетических заболеваний, всем будущим мамам рекомендуется генетическое обследование. А вот женщинам, входящим в группу риска, его провести следует в обязательном порядке. К группе риска относят:
- возрастные пары (когда одному или обоим партнерам более 35 лет);
- женщины, имеющие в анамнезе хроническое невынашивание плода;
- пары, у которых в роду рождались дети с генетическими отклонениями;
- пары, которые имеют детей с генетическими отклонениями;
- пары или один из будущих родителей, которые подверглись радиоизотопному облучению;
- и лица, имеющие патологическое пристрастие к алкоголю, наркотикам и даже табаку;
- женщин с поликистозными яичниками;
- бесплодием, причина которого неясна;
- будущих мам с неудачные попытками ЭКО в анамнезе;
- предыдущей и текущей осложненной беременностью.
Каждой паре, чтобы уточнить риск именно для них лучше пройти подобную проверку, потому, что для указанных групп генетический риск осложнений беременности и патологии плода значительно выше, чем для лиц, которые не подпадают под вышеперечисленные критерии.
Какие бывают генетические патологии?
Есть хромосомные мутации, на развитие которых современная медицина повлиять не может. И при выявлении высоких рисков женщине, если она уже вынашивает малыша, рекомендуют прерывание беременности.
Есть генетические дефекты организма матери, которые осложняют течение беременности, и, зная о которых акушер-гинеколог, ведущий беременность может постараться минимизировать последствия влияния таких отклонений.
Условно для удобства можно принять такое деление:
- генетические аномалии плода (синдромы Эдвардца, Дауна и другие);
- генетические дефекты организма матери, влияющие на течение беременности (мутации генов, которые приводят к тромбофилии, предрасположенность к гестозу, недостатку фолатов).
Деление условно, потому, что дефекты, отнесенные ко II группе, могут стать причиной аномалий плода, отнесенных к I группе. Но такое деление возможно, потому, что если выявить риски, относящиеся ко II группе, до зачатия и грамотно построить систему ведения беременности, есть шансы предотвратить и возникновение осложнений, и развитие аномалий плода.
Если обнаружена патология, относящаяся ко II группе генетических дефектов, то причины патологии плода в этом случае будут следующими:
- Тромбофилии (повышенная склонность к тромбообразованию), приводящие самоаборту в I триместре, к фетоплацентарной недостаточности и нарушению развития плода, даже его смерти на поздних сроках гестации. Повышенное тромбообразование часто становится причиной неудач ЭКО. В ряде случаев приводят к хромосомным аномалиям.
- Генетическая склонность к гестозам объясняется нарушением общего кровообращения. Это значит, что стенки сосудов будущей мамы имеют повышенную проницаемость. Именно это и приводит к основным симптомам гестоза. Тяжелые гестозы являются достаточно частой причиной гибели матери и ее малыша в перинатальном периоде. И их профилактику следует начинать со II триместра беременности. На сегодня медицинской науке известно более 30 генов, мутации которых, даже точечные приводят к повышению риска развития гестоза в несколько раз.
- Недостаток фолатов, приводит к аномалиям развития плода. Именно поэтому витамин В9 (фолиевую кислоту) рекомендуют принимать еще до зачатия, в период подготовки к беременности.
Выявление этих отклонений позволит разработать наиболее продуктивную тактику ведения беременности, и сохранить плод жизнеспособным до конца гестационного срока.
Предрасположенность матери к осложненному течению беременности лучше проверять до момента зачатия.
Пренатальный скрининг или тот самый анализ крови на патологию плода будущей маме предлагают сделать на 10-14 неделе гестационного процесса в сочетании со скрининговым УЗИ.
Источник: https://skoromamoy.ru/beremennost-i-plod/geneticheskiy-risk-oslozhneniy-beremennosti-i-patologii-ploda.html
Анализы в KDL. Генетический риск осложнений беременности и патологии плода

Данное исследование представляет собой выявление полиморфизмов в генах, связанных с наследственной тромбофилией и другими нарушениями системы свертывания крови, а также в генах, ответственных за обмен фолатов.
Мутации в исследуемых генах способны привести к различным осложнениям беременности, включая невынашивание, и патологиям развития плода, в связи с чем этот тест рекомендован всем женщинам, планирующим беременность.
Тромбофилия – это повышенная склонность к случайному (без видимых причин) тромбозу глубоких вен и тромбоэмболическим осложнениям.
Тромбоз может возникнуть при нарушениях кровообращения (застой крови), повышенной способности крови образовывать тромбы (гиперкоагуляции), повреждениях сосудистой стенки и при сочетании этих факторов.
Гиперкоагуляция может быть обусловлена наличием генетической предрасположенности к тромбофилии.
Фолатами называются соединения фолиевой кислоты (витамин B9), поступающие в организм с пищей. Они незаменимы для процессов, обеспечивающих физиологическое деление и нормальный рост всех клеток в организме, включая синтез нуклеотидов и репликацию ДНК.
В организме и естественные и синтетические фолаты с помощью ферментов фолатного цикла превращаются в активную форму – 5-метилтетрагидрофолат (5-МТГФ).
Это вещество необходимо для поддержания процесса метилирования ДНК, который обеспечивает стабильность генетической информации в клетках и правильную функцию генов.
При этом образуется гомоцистеин — вещество, повышение концентрации которого в крови служит фактором риска заболеваний сердца и сосудов, а также нарушений течения беременности у женщин (невынашивания, нарушений фетоплацентарного кровотока). Для обратного превращения гомоцистеина в метионин необходимо присутствие фолатов в организме в достаточном количестве.
Дефекты ферментов фолатного цикла связаны с повышенным риском повреждения сосудистой стенки за счет действия гомоцистеина и, соответственно, с риском развития сердечно- сосудистых событий как у мужчин, так и у женщин. У женщин наличие дефектов ферментов фолатного цикла может привести к низкому фолатному статусу, что служит причиной осложнений беременности, невынашивания, а также пороков развития плода
В каких случаях обычно назначают исследование?
Анализ рекомендован следующим категориям пациентов:
- Женщины, планирующие беременность
- Женщины с привычным невынашиванием беременности
- Женщины с осложненными предшествующими беременностями
- Родители (и мужчины, и женщины) в случае рождения ребенка с пороками развития плода (дефект нервной трубки, пороки сердца или урогенитального тракта)
- пациенты с семейной историей тромбофилии и других венозных осложнений (ВТЭО)
- пациенты с наличием в семейной истории сердечно- сосудистых событий (инфарктов и инсультов) у близких родственников в возрасте до 50 лет
Что именно определяется в процессе анализа?
В данном исследовании выявляются полиморфизмы следующих генов:
- F2 — ген протромбина.
- F5 – ген фактора V свертывания крови.
- F7 – ген проконвертина.
- F13A1 – ген, кодирующий A-субъединицу XIII фактора свертывания (F13A1).
- FGB – ген, кодирующий бета-субъединицу фибриногена.
- ITGA2 – ген, кодирующий тромбоцитарный гликопротеин Iа.
- ITGB3 – ген, кодирующий белок интегрин бета-3, являющийся компонентом тромбоцитарного гликопротеина IIb/IIIа.
- SERPINE1 (PAI-I) – ген ингибитора активатора плазминогена 1 типа.
- MTHFR – ген метилентетрагидрофолат-редуктазы.
- MTR – ген метионин-синтазы.
- MTRR – ген метионин-синтазы-редуктазы.
Что означают результаты теста?
В качестве заключения выдается генетическая карта здоровья, составленная профессиональным врачом-генетиком нашей лаборатории.
В ней представлены результаты анализа с расшифровкой, дано подробное описание исследуемых полиморфизмов и их влияния на риски развития тромбофилии, других нарушений системы свертывания крови, сердечно-сосудистых заболеваний, нарушений фолатного обмена и патологий беременности, советы по проведению дополнительных исследований и подробные клинические рекомендации для лечащего врача.
Результаты анализа интерпретируются лечащим врачом. Опираясь на них, врач может скорректировать питание и образ жизни пациента, назначить лекарственные препараты и дополнительные исследования.
Сроки выполнения теста
Результат генетического исследования можно получить спустя 10-11 дней после взятия крови.
Как подготовиться к анализу?
Следует придерживаться общих правил подготовки к взятию крови из вены. Кровь можно сдавать не ранее, чем через 3 часа после приема пищи в течение дня, или утром натощак. Чистую воду можно пить в обычном режиме.
Источник: https://kdl.ru/analizy-i-tseny/geneticheskiy-risk-oslozhneniy-beremennosti-i-patologii-ploda
Генетические факторы риска невынашивания и осложнений беременности. Исследование полиморфизмов в генах: F2 (20210 G>A), F5 R534Q G>A), MTHFR (E429A, A>C), MTHFR (A222V, C>T), FGB (455 G>A), SERPINE1 (–675 5G>4G), MTR (D919G, A>G), MTRR (I22M, A>G), ESR1 (T>C (PvuII)), ESR1 (A>G (XbaI)), AGT (M268T, T>C), TCF7L2 (IVS3, C>T)

array(19) { [«catalog_code»]=> string(6) «180036» [«name»]=> string(417) «Генетические факторы риска невынашивания и осложнений беременности.
Исследование полиморфизмов в генах: F2 (20210 G>A), F5 R534Q G>A), MTHFR (E429A, A>C), MTHFR (A222V, C>T), FGB (455 G>A), SERPINE1 (–675 5G>4G), MTR (D919G, A>G), MTRR (I22M, A>G), ESR1 (T>C (PvuII)), ESR1 (A>G (XbaI)), AGT (M268T, T>C), TCF7L2 (IVS3, C>T)» [«period»]=> string(1) «5» [«period_max»]=> string(2) «12» [«period_unit_name»]=> string(6) «к.д.» [«cito_period»]=> NULL [«cito_period_max»]=> NULL [«cito_period_unit_name»]=> NULL [«group_id»]=> string(6) «392581» [«id»]=> string(4) «3547» [«url»]=> string(78) «geneticheskije-faktory-riska-nevynashivanija-i-oslozhnenij-beremennosti-180036» [«podgotoa»]=> string(136) «
Не менее 3 часов после последнего приема пищи, можно пить воду без газа.
» [«opisanie»]=> string(16861) «
Метод исследования: Определение нуклеотидной последовательности соответствующих генетических локусов методом пиросеквенирования с использованием реагентов и оборудования фирмы Qiagen (Германия).
Невынашивание беременности — одна из самых актуальных проблем современного акушерства. Частота невынашивания беременности составляет от 10 до 25 % всех беременностей.
Одной из ведущих причин невынашивания беременности ранних сроков являются различные генетические факторы, причем помимо хромосомных перестроек невынашивание беременности может возникать как результат экспрессии функционально ослабленных вариантов (полиморфизмов) вышеперечисленных генов на фоне неблагоприятных внешних и внутренних факторов.
Выявление генетических полиморфизмов при планировании беременности позволяет минимизировать возможные опасные последствия, обусловленные индивидуальными генетическими особенностями женщины.
На сегодняшний день используется целая группа лекарственных препаратов еще на этапе планирования беременности (препараты, препятствующие агрегации тромбоцитов, антикоагулянты, полиненасыщенные жирные кислоты, антиоксиданты, фолиевая кислота и витаминно-минеральные комплексы), вероятность благополучного исхода беременности высока и при правильном и своевременном лечении достигает 95%.
В данной панели исследуются различные факторы, обусловливающие генетическую предрасположенность к невынашиванию и осложнениям беременности.
[attention type=green]Ген F2 кодирует протромбин (коагуляционный фактор II), ген F5 кодирует коагуляционный фактор V – оба белка являются ключевыми компонентами свертывающей системы крови.
[/attention]Вариации в данных генах обусловливают генетическую предрасположенность к повышенному тромбообразованию.
При наличии фактора риска в гене F2 повышен риск развития таких осложнений как невынашивание беременности, фетоплацентарная недостаточность, внутриутробная гибель плода, токсикоз, задержка развития плода и отслойка плаценты.
Наиболее опасным периодом в плане развития тромбозов глубоких вен во время беременности является конец второго — третий триместр и ранний послеродовый период. При наличии изменений в гене F5 повышен риск развития преэклампсии, отслойки нормально расположенной плаценты, ранней потери беременности, привычного невынашивания.
Определенную роль в невынашивании беременности могут играть гены, принимающие участие в метаболизме фолиевой кислоты и витамина В12. Высокие концентрации активной формы фолиевой кислоты необходимы для превращения гомоцистеина в метионин.
Основными генами, продукты которых контролируют превращение фолиевой кислоты в метаболически активные формы и регулируют обмен гомоцистеина, являются MTHFR(метилентетрагидрофолатредуктаза), MTRR (метионинсинтетазредуктаза), MTR (метионинредуктаза).
Полиморфизмы в этих генах связаны со снижением активности соответствующих ферментов и могут приводить к накоплению гомоцистеина.
Повышенный уровень гомоцистеина при беременности может приводить к нарушениям фетоплацентарного кровообращения, хронической гипоксии плода, задержке внутриутробного развития, преэклампсии, отслойки плаценты, развитию врожденного порока Spina bifida. При дополнительном действии других неблагоприятных факторов возможно самопроизвольное прерывание беременности на ранних сроках, в ряде случаев — привычное невынашивание беременности.
Ген FGB кодирует фибриноген — белок, предшественник фибрина, присутствующий в плазме крови.
Под влиянием фермента тромбина из фибриногена образуется нерастворимый белок фибрин на заключительном этапе свертывания крови, что образует основу фибринового тромба.
Исследуемая вариация в гене FGB ассоциирована с повышением уровня фибриногена плазмы крови, и, как следствие, повышением риска развития преэклампсии, отслойки нормально расположенной плаценты и развития акушерских осложнений.
[attention type=yellow]Изменение гена SERPINE1 приводит к повышению концентрации белка ингибитора активатора плазминогена и обусловливает повышенную склонность к тромбозу.
[/attention]Наличие фактора риска связано с повышенным риском отслойки хориона и плаценты в ранние сроки беременности и, по некоторым литературным данным, с повышенным риском ранней потери беременности, особенно в сочетании с дополнительными отягощающими факторами.
Ген ESR1 кодирует рецептор эстрогена альфа. Гормон участвует в регуляции полового развития, гаметогенеза, роста и поддержания скелета, функционировании сердечно-сосудистой и нервной систем.
Изменения гена приводят к снижению выработки эстрогенового рецептора, вызывая риск невынашивания беременности, акушерских осложнений, а полиморфизм T>C (PvuII), кроме того, дает неблагоприятный прогноз для осуществления ЭКО.
Полиморфизм в гене AGT, кодирующем ангиотензиноген, приводит к повышению концентрации ангиотензиногена в крови, повышая риск развития преэклампсии во время беременности. У женщин — носителей аллеля риска С повышен риск развития инфаркта миокарда и других сердечно — сосудистых событий на фоне гормоно-заместительной терапии (ГЗТ).
Гестационный диабет – повышенное содержание глюкозы в крови, возникающее во время беременности. При возникновении гестационного сахарного диабета на начальных сроках беременности значительно возрастает риск самопроизвольного аборта, врожденных пороков развития сердца и мозговых структур плода.
На поздних сроках (2-3й триместры), гестационный диабет приводит к чрезмерному росту плода (макросомии) и гиперинсулинемии, а после рождения может проявиться заболеванием внутренних органов плода (диабетической фетопатией). Ген TCF7L2 кодирует фактор, регулирующий рост, деление и развитие клеток поджелудочной железы.
Исследуемый генетический вариант ассоциирован с повышенным риском развития гестационного диабета (диабета беременных).
Показания к исследованию:
- Всем женщинам при плановой подготовке к беременности;
- При наличии в анамнезе двух и более прерываний беременности на ранних сроках, тяжёлых осложнений беременности (гестоз, задержка развития плода, внутриутробная гибель плода), неудачных попытках ЭКО;
- При назначении оральных гормональных контрацептивов, заместительной гормональной терапии (при выявлении генетической предрасположенности к тромбозам назначение данной категории препаратов противопоказано!);
- При подготовке к ЭКО;
- При низком уровне половых гормонов (эстрогенов).
Интерпретация результатов:
Пример результата исследования. Генетические факторы риска невынашивания и осложнений беременности
| Полиморфизм в гене F2 (протромбин, 20210 G>A), rs1799963 | GG |
| Полиморфизм в гене F5 (коагуляционный фактор V, мутация Лейдена, R534Q G>A), rs6025 | GG |
| Полиморфизм в гене MTHFR (метилентетрагидрофолатредуктаза, E429A, A>C) rs1801131 | AA |
| Полиморфизм в гене MTHFR (метилентетрагидрофолатредуктаза, A222V, C>T), rs1801133 | TT |
| Полиморфизм в гене FGB (фибриноген, 455 G>A) rs1800790 | AA |
| Полиморфизм в гене SERPINE1 (ингибитор активатора плазминогена 1, –675 5G>4G, rs1799768) | 5G/5G |
| Полиморфизм в гене MTR (Метионинсинтаза, D919G, A>G) rs1805087 | AA |
| Полиморфизм в гене MTRR (Метионинсинтазаредуктаза, I22M, A>G) rs1801394 | AA |
| Полиморфизм в гене ESR1 (Эстрогеновый рецептор, T>C (PvuII)), rs2234693 | TС |
| Полиморфизм в гене ESR1 (Эстрогеновый рецептор, A>G (XbaI)) rs9340799 | AG |
| Полиморфизм в гене AGT (Ангиотензиноген, M268T, T>C), rs699 | CC |
| Полиморфизм в гене TCF7L2 (Фактор транскрипции 7, IVS3 C>T) rs7903146 | CC |
Источник: https://www.cmd-online.ru/analizy-i-tseny/geneticheskije-faktory-riska-nevynashivanija-i-oslozhnenij-beremennosti-180036/